

近日,海博为药业在创新药研发领域迎来关键里程碑 —— 公司首款自主创新药 HBW-3220 胶囊的 Ⅲ 期临床试验方案,已顺利通过国家药品监督管理局药品审评中心(CDE)评审。这一突破性进展标志着 HBW-3220 胶囊正式迈入 关键性Ⅲ 期临床研究阶段,也为海博为药业打通 “创新研发到市场价值转化” 的关键链路,开启了企业发展的全新篇章。
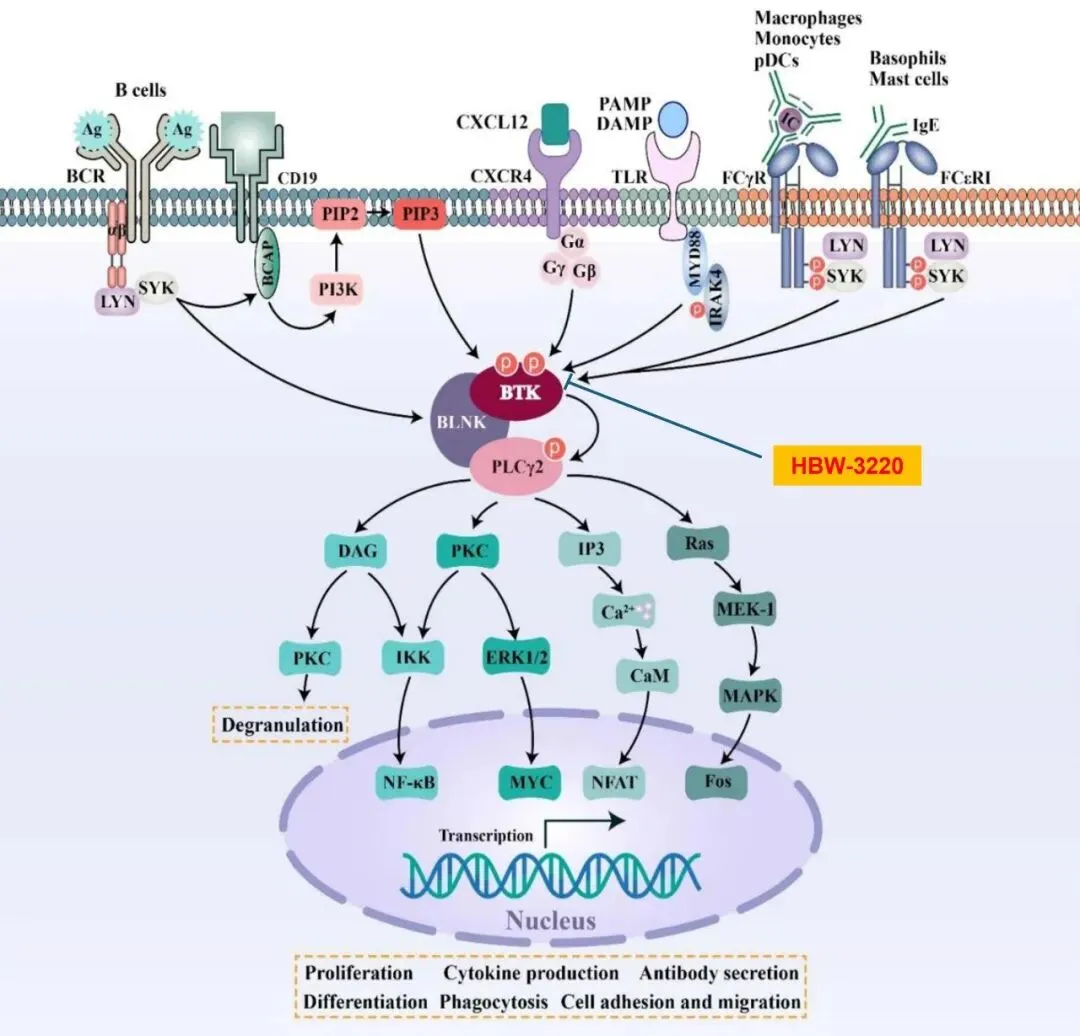
作为海博为药业自主研发的核心成果,HBW-3220 胶囊凭借 “可逆、非共价” 的分子设计与 “四代 BTK 抑制剂” 的技术定位,从根源上破解了当前 BTK 抑制剂治疗领域的核心痛点 ——耐药难题。相较于前三代 BTK 抑制剂普遍受制于 C481S 突变耐药的局限,HBW-3220 胶囊实现了 “跨代突破”:不仅能高效克服 C481S 突变耐药,更对临床中新出现的 L528W、T474I 等多种耐药突变展现出优异的抑制效果,为B细胞淋巴瘤患者提供更多优质的用药选择,有望填补全球百亿级 BTK 抑制剂后续治疗市场的空白。
更值得关注的是,已完成的Ⅰ/II 期临床研究充分印证了HBW-3220 胶囊在安全性与有效性上的双重优势,显著优于当前已上市同类药物,开发潜力巨大。
作为治疗 B 细胞淋巴瘤的 “主力药物品类”,BTK 抑制剂市场仍在持续扩容。据弗若斯特沙利文数据预测,2030 年全球 BTK 抑制剂市场规模将攀升至 261 亿美元,市场空间广阔。HBW-3220 胶囊的价值也远不止于肿瘤治疗领域,该药还获得了新增适应症(肾小球肾炎)的临床批件,在自身免疫性疾病领域也有深厚的开发潜力,未来有望打造 “肿瘤 + 自免” 双赛道布局,进一步打开市场增长天花板。
目前,海博为药业已完成临床研究队伍升级,将以 “全速推进” 的节奏推动 HBW-3220 胶囊在B细胞淋巴瘤适应症上的 Ⅲ 期临床研究,加速项目的产业化进程,为全球患者带来新的治疗曙光。
来源:海博为药业